黑政辦發(fā)〔2021〕43號
字號: 大 中 小
各市(地)、縣(市)人民政府(行署),省政府各直屬單位:
《黑龍江省全面加強藥品監(jiān)管能力建設的若干措施》已經(jīng)省政府同意,現(xiàn)印發(fā)給你們,請認真抓好貫徹落實。
黑龍江省人民政府辦公廳
2021年12月30日
黑龍江省全面加強
藥品監(jiān)管能力建設的若干措施
為貫徹落實《國務院辦公廳關于全面加強藥品監(jiān)管能力建設的實施意見》(國辦發(fā)〔2021〕16號),全面加強藥品監(jiān)管能力建設,現(xiàn)結(jié)合我省實際提出如下措施。
一、總體要求
以習近平新時代中國特色社會主義思想為指導,全面貫徹黨的十九大和十九屆歷次全會精神和習近平總書記在深入推進東北振興座談會上的重要講話以及對我省重要講話重要指示批示精神,切實增強“四個意識”、堅定“四個自信”、做到“兩個維護”。堅持人民至上、生命至上,認真落實黨中央、國務院和國家藥監(jiān)局以及省委、省政府決策部署,落實“四個最嚴”要求,強基礎、補短板、破瓶頸、促提升,不斷創(chuàng)新藥品監(jiān)管方式方法,加快建立更加科學、高效、權威的藥品監(jiān)管體系,堅決守住藥品安全底線,進一步提升藥品監(jiān)管工作科學化、法治化、國際化、現(xiàn)代化水平,更好保護和促進人民群眾身體健康,促進醫(yī)藥產(chǎn)業(yè)高質(zhì)量發(fā)展。
二、工作措施
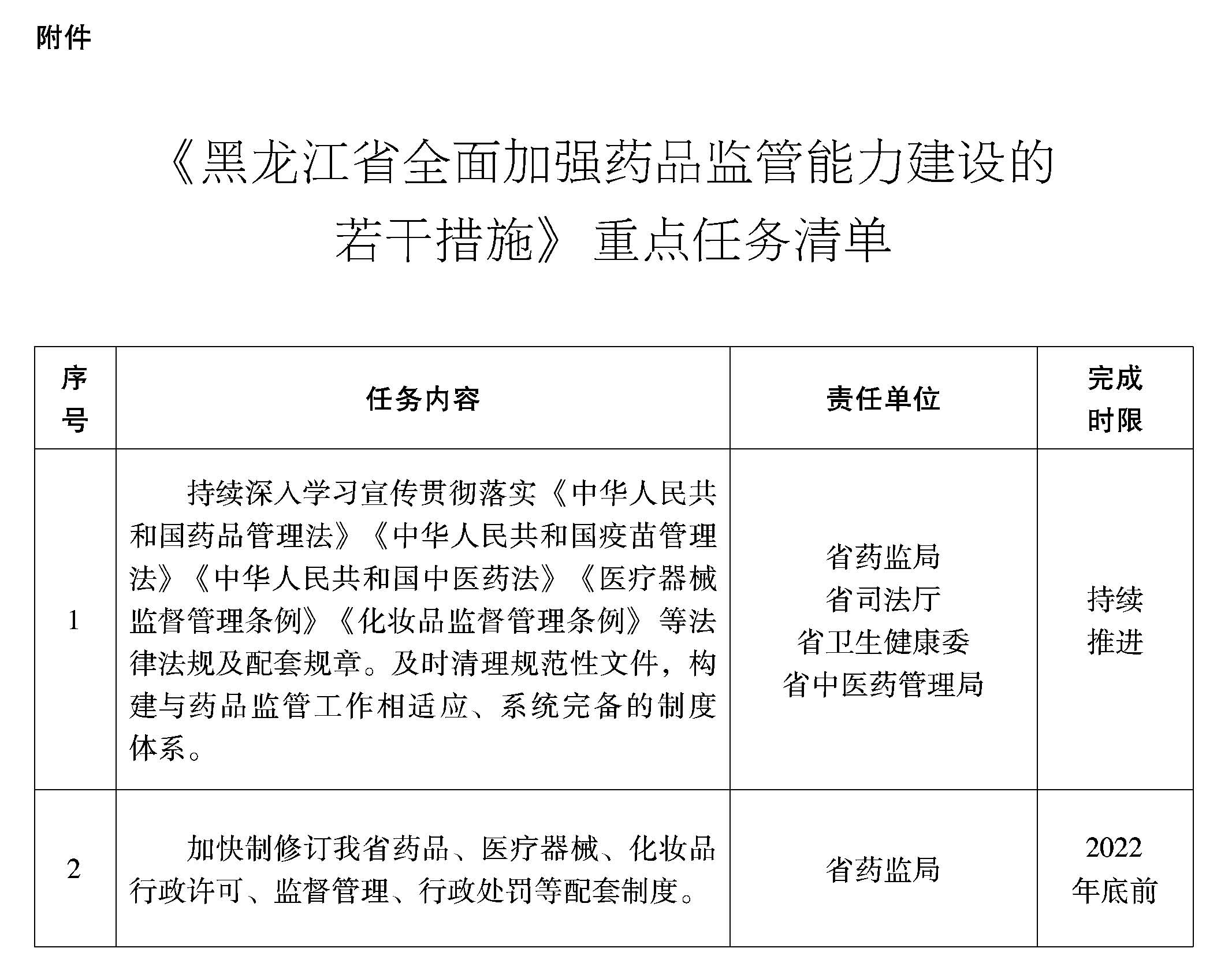
(一)健全法規(guī)制度體系。持續(xù)深入學習宣傳貫徹落實《中華人民共和國藥品管理法》《中華人民共和國疫苗管理法》《中華人民共和國中醫(yī)藥法》《醫(yī)療器械監(jiān)督管理條例》《化妝品監(jiān)督管理條例》等法律法規(guī)及配套規(guī)章,加快制修訂我省藥品、醫(yī)療器械、化妝品的行政許可、監(jiān)督管理、行政處罰等配套制度,及時清理規(guī)范性文件,構(gòu)建與藥品監(jiān)管工作相適應、系統(tǒng)完備的制度體系。
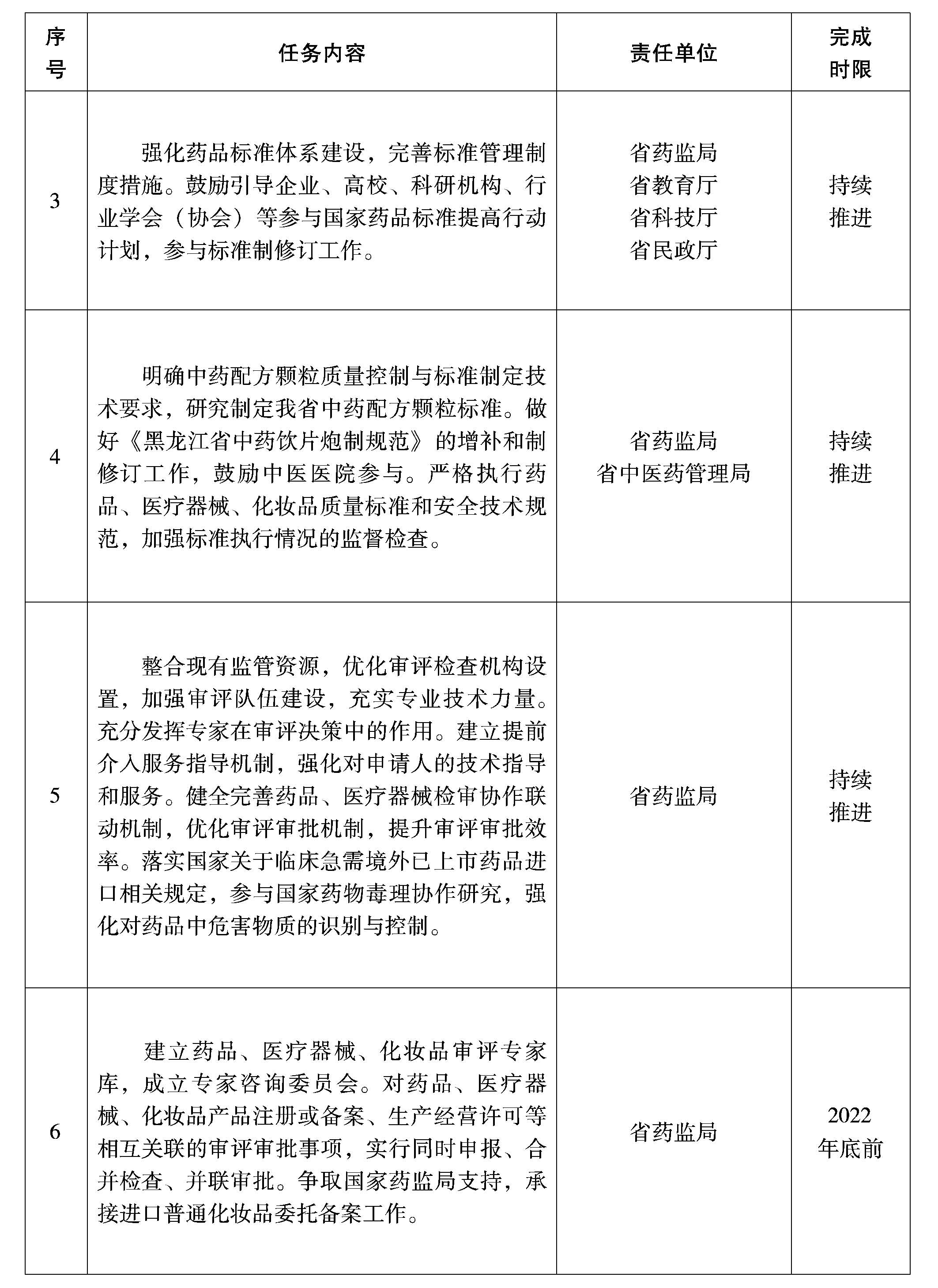
(二)嚴格標準管理與執(zhí)行。強化藥品標準體系建設,完善標準管理制度措施。鼓勵引導企業(yè)、高校、科研機構(gòu)、行業(yè)學會(協(xié)會)等參與國家藥品標準提高行動計劃,參與標準制修訂工作。明確中藥配方顆粒質(zhì)量控制與標準制定技術要求,研究制定我省中藥配方顆粒標準。做好《黑龍江省中藥飲片炮制規(guī)范》的增補和制修訂工作,鼓勵中醫(yī)醫(yī)院參與。嚴格執(zhí)行藥品、醫(yī)療器械、化妝品質(zhì)量標準和安全技術規(guī)范,加強標準執(zhí)行情況的監(jiān)督檢查。
(三)提高審評審批能力。整合現(xiàn)有監(jiān)管資源,優(yōu)化審評檢查機構(gòu)設置,加強審評隊伍建設,充實專業(yè)技術力量。建立藥品、醫(yī)療器械、化妝品審評專家?guī)欤闪<易稍兾瘑T會,充分發(fā)揮專家在審評決策中的作用。建立提前介入服務指導機制,強化對申請人的技術指導和服務。對藥品、醫(yī)療器械、化妝品產(chǎn)品注冊或備案、生產(chǎn)經(jīng)營許可等相互關聯(lián)的審評審批事項,實行同時申報、合并檢查、并聯(lián)審批。健全完善藥品、醫(yī)療器械檢審協(xié)作聯(lián)動機制,優(yōu)化審評審批機制,提升審評審批效率。爭取國家藥監(jiān)局支持,承接進口普通化妝品委托備案工作。落實國家關于臨床急需境外已上市藥品進口相關規(guī)定,參與國家藥物毒理協(xié)作研究,強化對藥品中危害物質(zhì)的識別與控制。
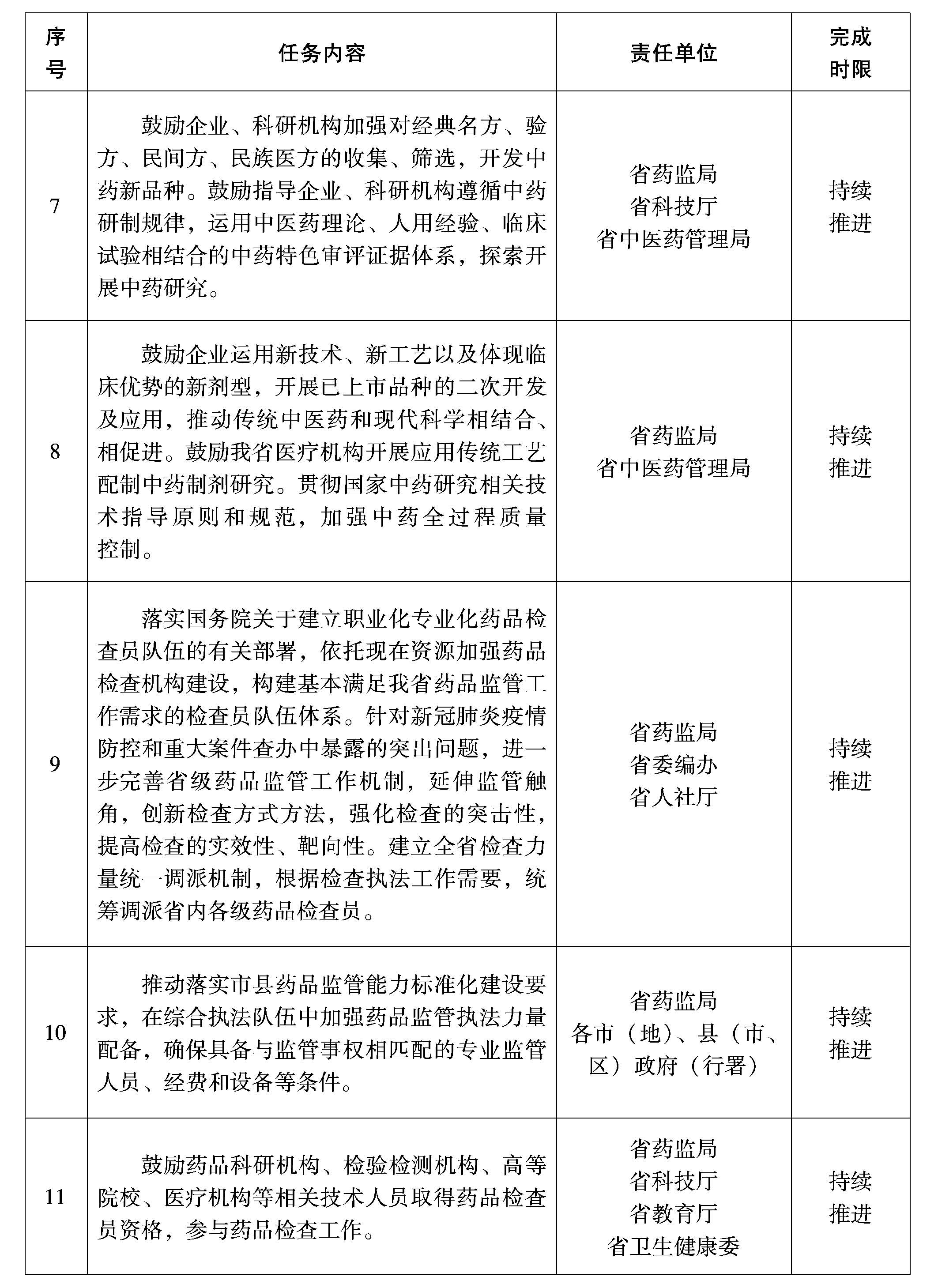
(四)提升中藥傳承創(chuàng)新能力。鼓勵企業(yè)、科研機構(gòu)加強對經(jīng)典名方、驗方、民間方、民族醫(yī)方的收集、篩選,開發(fā)中藥新品種。鼓勵指導企業(yè)、科研機構(gòu)遵循中藥研制規(guī)律,運用中醫(yī)藥理論、人用經(jīng)驗、臨床試驗相結(jié)合的中藥特色審評證據(jù)體系,探索開展中藥研究。鼓勵企業(yè)運用新技術、新工藝以及體現(xiàn)臨床優(yōu)勢的新劑型,開展已上市品種的二次開發(fā)及應用,推動傳統(tǒng)中醫(yī)藥和現(xiàn)代科學相結(jié)合、相促進。鼓勵我省醫(yī)療機構(gòu)開展應用傳統(tǒng)工藝配制中藥制劑研究。貫徹國家中藥研究相關技術指導原則和規(guī)范,加強中藥全過程質(zhì)量控制,優(yōu)化醫(yī)療機構(gòu)中藥制劑管理。
(五)健全檢查執(zhí)法體系。落實國務院關于建立職業(yè)化專業(yè)化藥品檢查員隊伍的有關部署,依托現(xiàn)有資源加強藥品檢查機構(gòu)建設,構(gòu)建基本滿足我省藥品監(jiān)管工作需求的檢查員隊伍體系。針對新冠肺炎疫情防控和重大案件查辦中暴露的突出問題,進一步完善省級藥品監(jiān)管工作機制,延伸監(jiān)管觸角,創(chuàng)新檢查方式方法,強化檢查的突擊性,提高檢查的實效性、靶向性。推動落實市縣藥品監(jiān)管能力標準化建設要求,在綜合執(zhí)法隊伍中加強藥品監(jiān)管執(zhí)法力量配備,確保具備與監(jiān)管事權相匹配的專業(yè)監(jiān)管人員、經(jīng)費和設備等條件。建立全省檢查力量統(tǒng)一調(diào)派機制,根據(jù)檢查執(zhí)法工作需要,統(tǒng)籌調(diào)派省內(nèi)各級藥品檢查員。鼓勵藥品科研機構(gòu)、檢驗檢測機構(gòu)、高等院校、醫(yī)療機構(gòu)等相關技術人員取得藥品檢查員資格,參與藥品檢查工作。
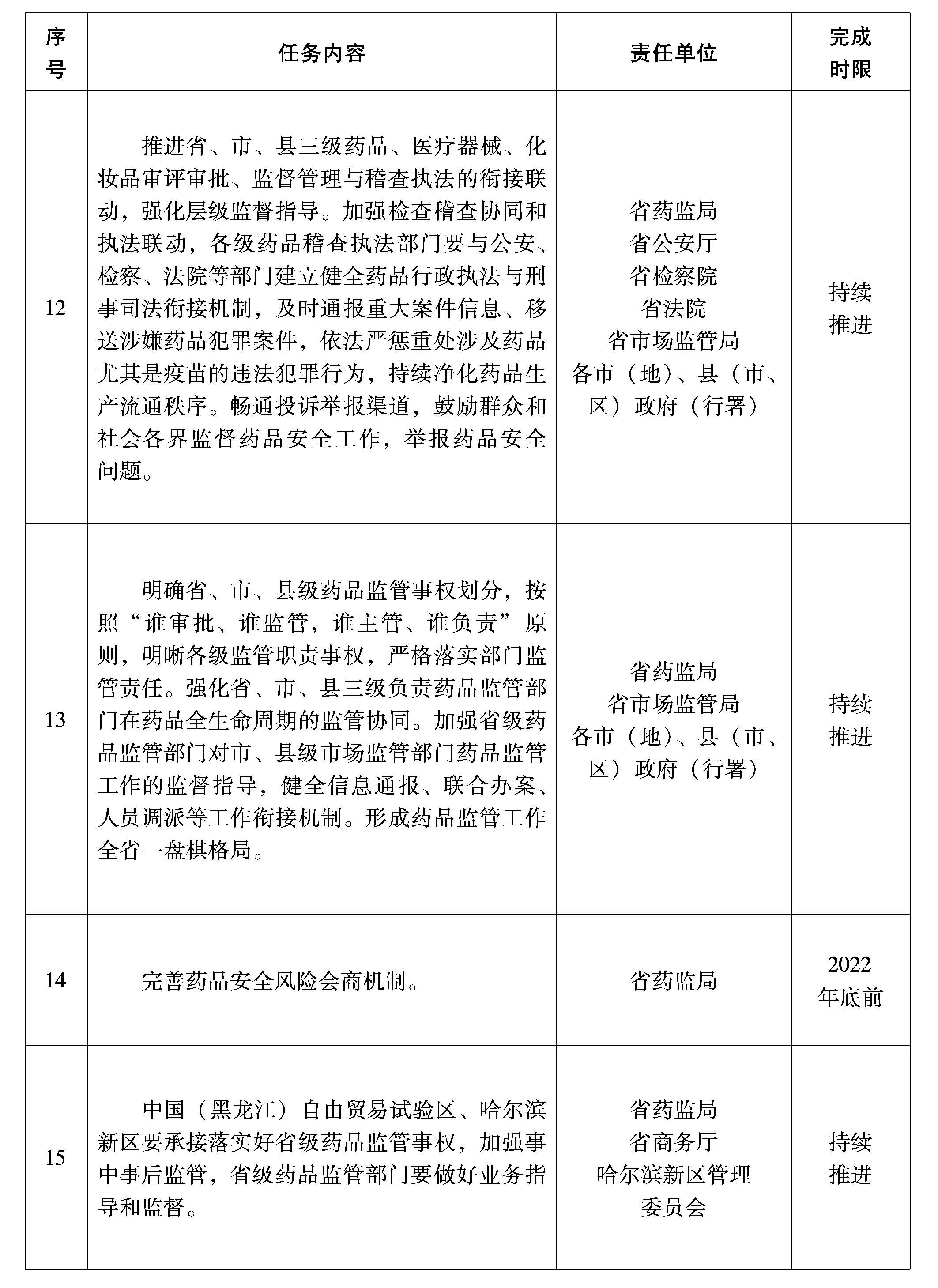
(六)提升稽查辦案效能。推進省、市、縣三級藥品、醫(yī)療器械、化妝品審評審批、監(jiān)督管理與稽查執(zhí)法的銜接聯(lián)動,強化層級監(jiān)督指導。加強檢查稽查協(xié)同和執(zhí)法聯(lián)動,各級藥品稽查執(zhí)法部門要與公安、檢察、法院等部門建立健全藥品行政執(zhí)法與刑事司法銜接機制,及時通報重大案件信息、移送涉嫌犯罪案件,依法嚴懲重處涉及藥品尤其是疫苗的違法犯罪行為,持續(xù)凈化藥品生產(chǎn)流通秩序。暢通投訴舉報渠道,鼓勵群眾和社會各界監(jiān)督藥品安全工作,舉報藥品安全問題。
(七)強化監(jiān)管部門協(xié)同。明確省、市、縣級藥品監(jiān)管事權劃分,按照“誰審批、誰監(jiān)管,誰主管、誰負責”原則,明晰各級監(jiān)管職責事權,嚴格落實部門監(jiān)管責任。強化省、市、縣三級負責藥品監(jiān)管部門在藥品全生命周期的監(jiān)管協(xié)同。加強省級藥品監(jiān)管部門對市、縣級市場監(jiān)管部門藥品監(jiān)管工作的監(jiān)督指導,健全信息通報、聯(lián)合辦案、人員調(diào)派等工作銜接機制,完善藥品安全風險會商機制,形成藥品監(jiān)管工作全省一盤棋格局。中國(黑龍江)自由貿(mào)易試驗區(qū)、哈爾濱新區(qū)要承接落實好省級藥品監(jiān)管事權,加強事中事后監(jiān)管,省級藥品監(jiān)管部門要做好業(yè)務指導和監(jiān)督。
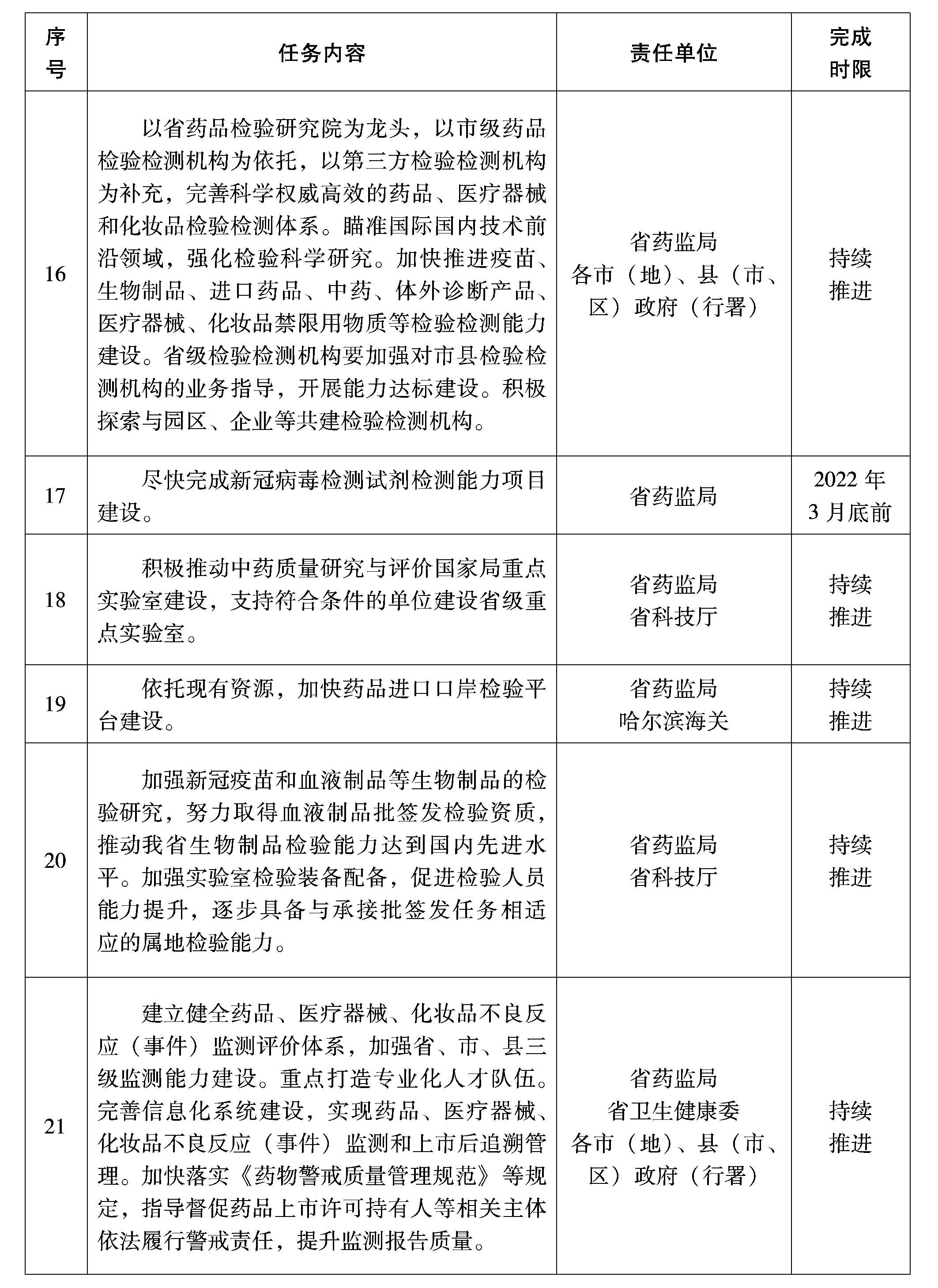
(八)提升檢驗檢測能力。以省藥品檢驗研究院為龍頭,以市級藥品檢驗檢測機構(gòu)為依托,以第三方檢驗檢測機構(gòu)為補充,完善科學權威高效的藥品、醫(yī)療器械和化妝品檢驗檢測體系。瞄準國際國內(nèi)技術前沿領域,強化檢驗科學研究。積極推動國家藥監(jiān)局中藥質(zhì)量研究與評價重點實驗室建設,支持符合條件的單位建設省級重點實驗室。加快推進疫苗、生物制品、進口藥品、中藥、體外診斷產(chǎn)品、醫(yī)療器械、化妝品禁限用物質(zhì)等檢驗檢測能力建設。依托現(xiàn)有資源,加快藥品進口口岸檢驗平臺建設,積極探索與園區(qū)、企業(yè)等共建檢驗檢測機構(gòu)。省級檢驗檢測機構(gòu)要加強對市、縣級檢驗檢測機構(gòu)的業(yè)務指導,開展能力達標建設。盡快完成新冠病毒檢測試劑檢測能力項目建設。優(yōu)化檢驗檢測程序,支持藥品、醫(yī)療器械和化妝品領域的科技創(chuàng)新和產(chǎn)業(yè)發(fā)展。
(九)提升生物制品(疫苗)批簽發(fā)能力。加強新冠疫苗和血液制品等生物制品的檢驗研究,努力取得血液制品批簽發(fā)檢驗資質(zhì),推動我省生物制品檢驗能力達到國內(nèi)先進水平。加強實驗室檢驗裝備配備,促進檢驗人員能力提升,逐步具備與承接批簽發(fā)任務相適應的屬地檢驗能力。
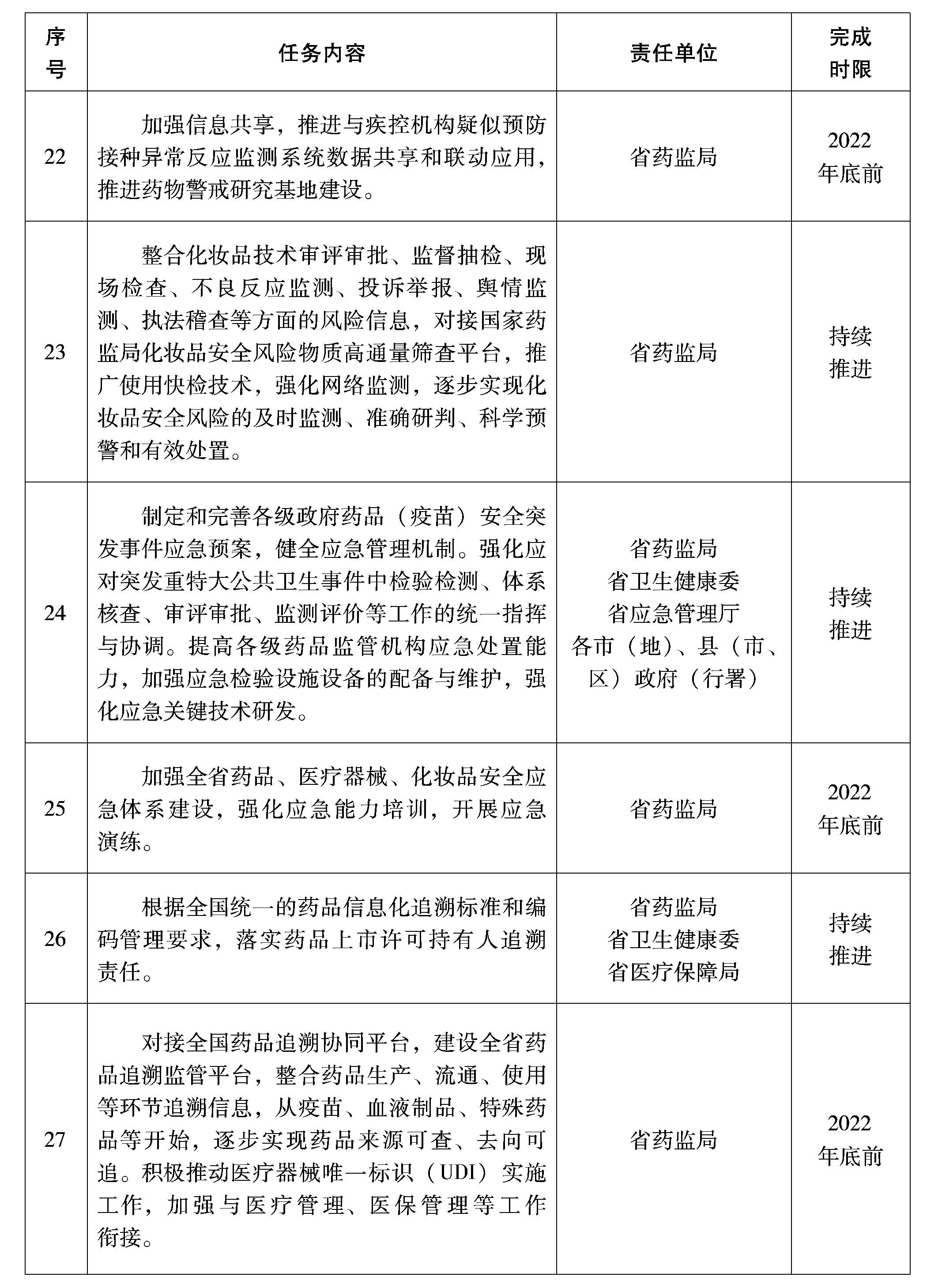
(十)建立完善藥物警戒體系。建立健全藥品、醫(yī)療器械、化妝品不良反應(事件)監(jiān)測評價體系,加強省、市、縣三級監(jiān)測能力建設。重點打造專業(yè)化人才隊伍。完善信息化系統(tǒng)建設,實現(xiàn)藥品、醫(yī)療器械、化妝品不良反應(事件)監(jiān)測和上市后追溯管理。加強信息共享,推進與疾控機構(gòu)疑似預防接種異常反應監(jiān)測系統(tǒng)數(shù)據(jù)共享和聯(lián)動應用。推進藥物警戒研究基地建設,加快落實《藥物警戒質(zhì)量管理規(guī)范》等規(guī)定,指導督促藥品上市許可持有人等相關主體依法履行警戒責任,提升監(jiān)測報告質(zhì)量。
(十一)提升化妝品風險防控能力。整合化妝品技術審評審批、監(jiān)督抽檢、現(xiàn)場檢查、不良反應監(jiān)測、投訴舉報、輿情監(jiān)測、執(zhí)法稽查等方面的風險信息,對接國家藥監(jiān)局化妝品安全風險物質(zhì)高通量篩查平臺,推廣使用快檢技術,強化網(wǎng)絡監(jiān)測,逐步實現(xiàn)化妝品安全風險的及時監(jiān)測、準確研判、科學預警和有效處置。
(十二)健全應急管理機制。制定和完善各級政府藥品(疫苗)安全突發(fā)事件應急預案,健全應急管理機制。強化應對突發(fā)重特大公共衛(wèi)生事件中檢驗檢測、體系核查、審評審批、監(jiān)測評價等工作的統(tǒng)一指揮與協(xié)調(diào)。加強全省藥品、醫(yī)療器械、化妝品安全應急體系建設,強化應急能力培訓,開展應急演練,提高各級藥品監(jiān)管機構(gòu)應急處置能力。加強應急檢驗設施設備的配備與維護,強化應急關鍵技術研發(fā)。
(十三)加快信息化追溯體系建設。根據(jù)全國統(tǒng)一的藥品信息化追溯標準和編碼管理要求,落實藥品上市許可持有人追溯責任。對接全國藥品追溯協(xié)同平臺,建設全省藥品追溯監(jiān)管平臺,整合藥品生產(chǎn)、流通、使用等環(huán)節(jié)追溯信息,從疫苗、血液制品、特殊藥品等開始,逐步實現(xiàn)藥品來源可查、去向可追。積極推動醫(yī)療器械唯一標識(UDI)實施工作,加強與醫(yī)療管理、醫(yī)保管理等工作銜接,確保醫(yī)用耗材唯一標識與醫(yī)保部門醫(yī)用耗材分類與代碼的編碼規(guī)則和方法一致。
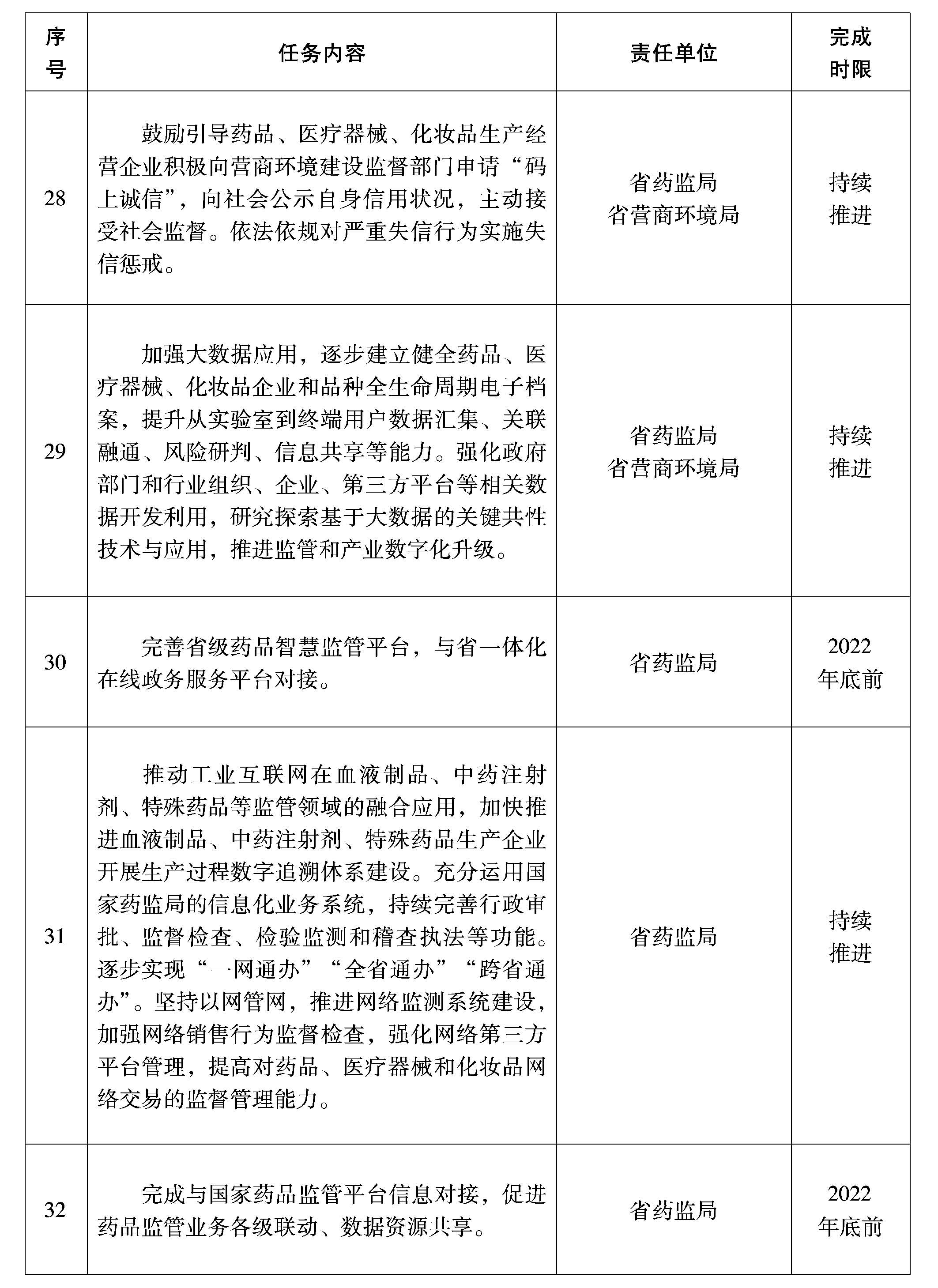
(十四)推進全生命周期數(shù)字化管理。加強大數(shù)據(jù)應用,逐步建立健全藥品、醫(yī)療器械、化妝品企業(yè)和品種全生命周期電子檔案,提升從實驗室到終端用戶數(shù)據(jù)匯集、關聯(lián)融通、風險研判、信息共享等能力。完善省級藥品智慧監(jiān)管平臺,與省一體化在線政務服務平臺對接。強化政府部門和行業(yè)組織、企業(yè)、第三方平臺等相關數(shù)據(jù)開發(fā)利用,研究探索基于大數(shù)據(jù)的關鍵共性技術與應用,推進監(jiān)管和產(chǎn)業(yè)數(shù)字化升級。鼓勵引導藥品、醫(yī)療器械、化妝品生產(chǎn)經(jīng)營企業(yè)積極向營商環(huán)境建設監(jiān)督部門申請“碼上誠信”,向社會公示自身信用狀況,主動接受社會監(jiān)督。依法依規(guī)對嚴重失信行為實施失信懲戒。
(十五)提升“互聯(lián)網(wǎng)+藥品監(jiān)管”水平。推動工業(yè)互聯(lián)網(wǎng)在血液制品、中藥注射劑、特殊藥品等監(jiān)管領域的融合應用。充分運用國家藥監(jiān)局的信息化業(yè)務系統(tǒng),持續(xù)完善行政審批、監(jiān)督檢查、檢驗監(jiān)測和稽查執(zhí)法等功能。完成與國家藥品監(jiān)管平臺信息對接,促進藥品監(jiān)管業(yè)務各級聯(lián)動、數(shù)據(jù)資源共享,逐步實現(xiàn)“一網(wǎng)通辦”“全省通辦”“跨省通辦”。堅持以網(wǎng)管網(wǎng),推進網(wǎng)絡監(jiān)測系統(tǒng)建設,加強網(wǎng)絡銷售行為監(jiān)督檢查,強化網(wǎng)絡第三方平臺管理,提高對藥品、醫(yī)療器械和化妝品網(wǎng)絡交易的監(jiān)督管理能力。
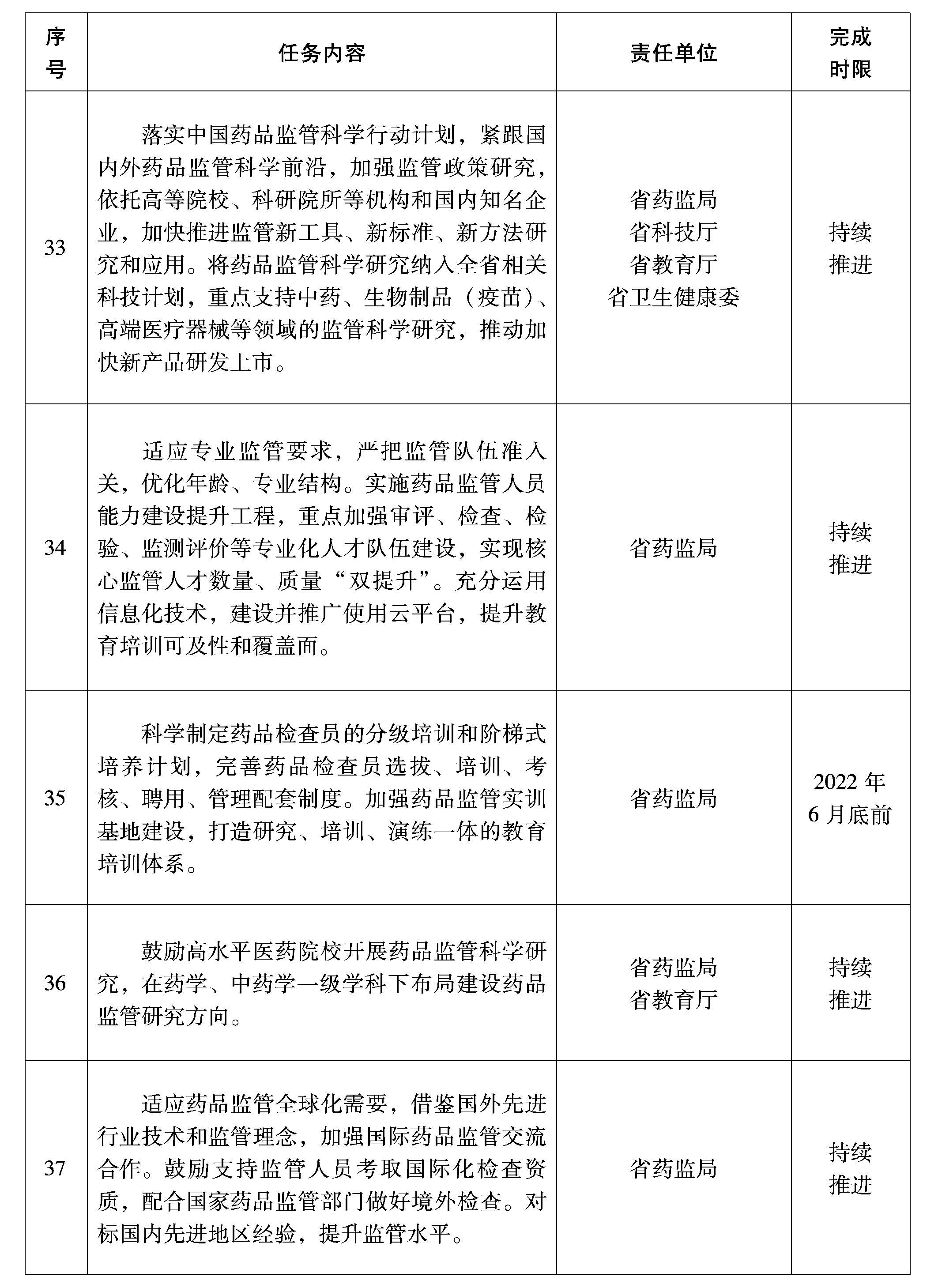
(十六)實施藥品監(jiān)管科學行動計劃。落實中國藥品監(jiān)管科學行動計劃,緊跟國內(nèi)外藥品監(jiān)管科學前沿,加強監(jiān)管政策研究,依托高等院校、科研院所等機構(gòu)和國內(nèi)知名企業(yè),加快推進監(jiān)管新工具、新標準、新方法研究和應用。將藥品監(jiān)管科學研究納入全省相關科技計劃,重點支持中藥、生物制品(疫苗)、高端醫(yī)療器械等領域的監(jiān)管科學研究,推動加快新產(chǎn)品研發(fā)上市。
(十七)提升監(jiān)管隊伍素質(zhì)。適應專業(yè)監(jiān)管要求,嚴把監(jiān)管隊伍準入關,優(yōu)化年齡、專業(yè)結(jié)構(gòu)。實施藥品監(jiān)管人員能力建設提升工程,重點加強審評、檢查、檢驗、監(jiān)測評價等專業(yè)化人才隊伍建設,實現(xiàn)核心監(jiān)管人才數(shù)量、質(zhì)量“雙提升”。科學制定藥品檢查員的分級培訓和階梯式培養(yǎng)計劃,完善藥品檢查員選拔、培訓、考核、聘用、管理配套制度。加強藥品監(jiān)管實訓基地建設,打造研究、培訓、演練一體的教育培訓體系。充分運用信息化技術,建設并推廣使用云平臺,提升教育培訓可及性和覆蓋面。鼓勵高水平醫(yī)藥院校開展藥品監(jiān)管人才培養(yǎng)和科學研究,在藥學、中藥學一級學科下布局建設藥品監(jiān)管研究方向。
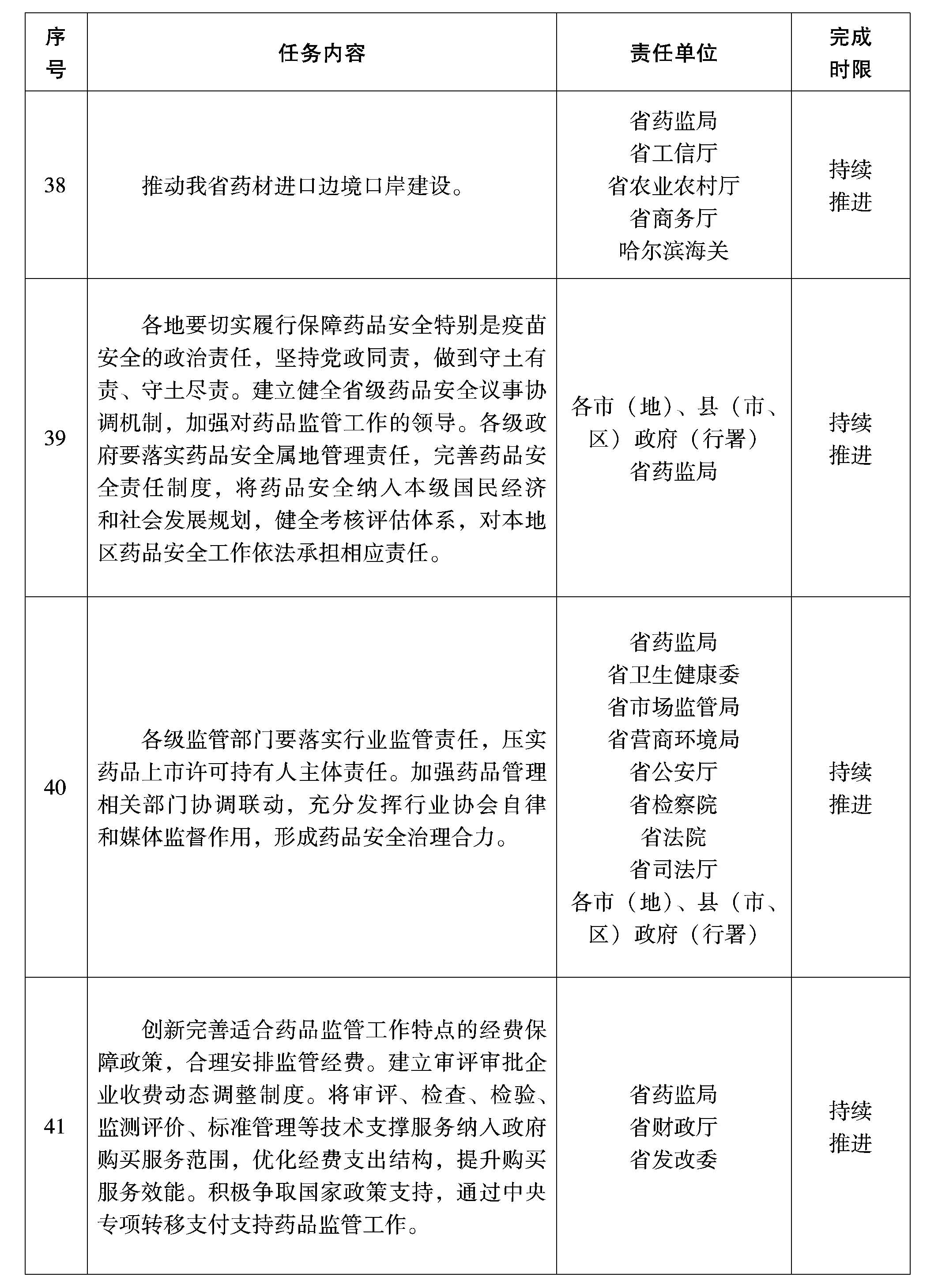
(十八)對標國際國內(nèi)先進提升監(jiān)管水平。適應藥品監(jiān)管全球化需要,借鑒國外先進行業(yè)技術和監(jiān)管理念,加強國際藥品監(jiān)管交流合作。推動我省藥材進口邊境口岸建設。鼓勵支持監(jiān)管人員考取國際化檢查資質(zhì),配合國家藥品監(jiān)管部門做好境外檢查。對標國內(nèi)先進地區(qū)經(jīng)驗,提升監(jiān)管水平。
三、保障措施
(十九)加強組織領導。各地要切實履行保障藥品安全特別是疫苗安全的政治責任,堅持黨政同責,做到守土有責、守土盡責。建立省級藥品安全議事協(xié)調(diào)機制,加強對藥品監(jiān)管工作的領導。各級政府要落實藥品安全屬地管理責任,完善藥品安全責任制度,將藥品安全納入本級國民經(jīng)濟和社會發(fā)展規(guī)劃,健全考核評估體系,對本地區(qū)藥品安全工作依法承擔相應責任。
(二十)完善治理機制。各級監(jiān)管部門要落實行業(yè)監(jiān)管責任,壓實藥品上市許可持有人主體責任。加強藥品管理相關部門協(xié)調(diào)聯(lián)動,充分發(fā)揮行業(yè)協(xié)會自律和媒體監(jiān)督作用,形成藥品安全治理合力。
(二十一)強化政策保障。創(chuàng)新完善適合藥品監(jiān)管工作特點的經(jīng)費保障政策,合理安排監(jiān)管經(jīng)費。建立審評審批企業(yè)收費動態(tài)調(diào)整制度。將審評、檢查、檢驗、監(jiān)測評價、標準管理等技術支撐服務納入政府購買服務范圍,優(yōu)化經(jīng)費支出結(jié)構(gòu),提升購買服務效能。積極爭取國家政策支持,通過中央專項轉(zhuǎn)移支付支持藥品監(jiān)管工作。
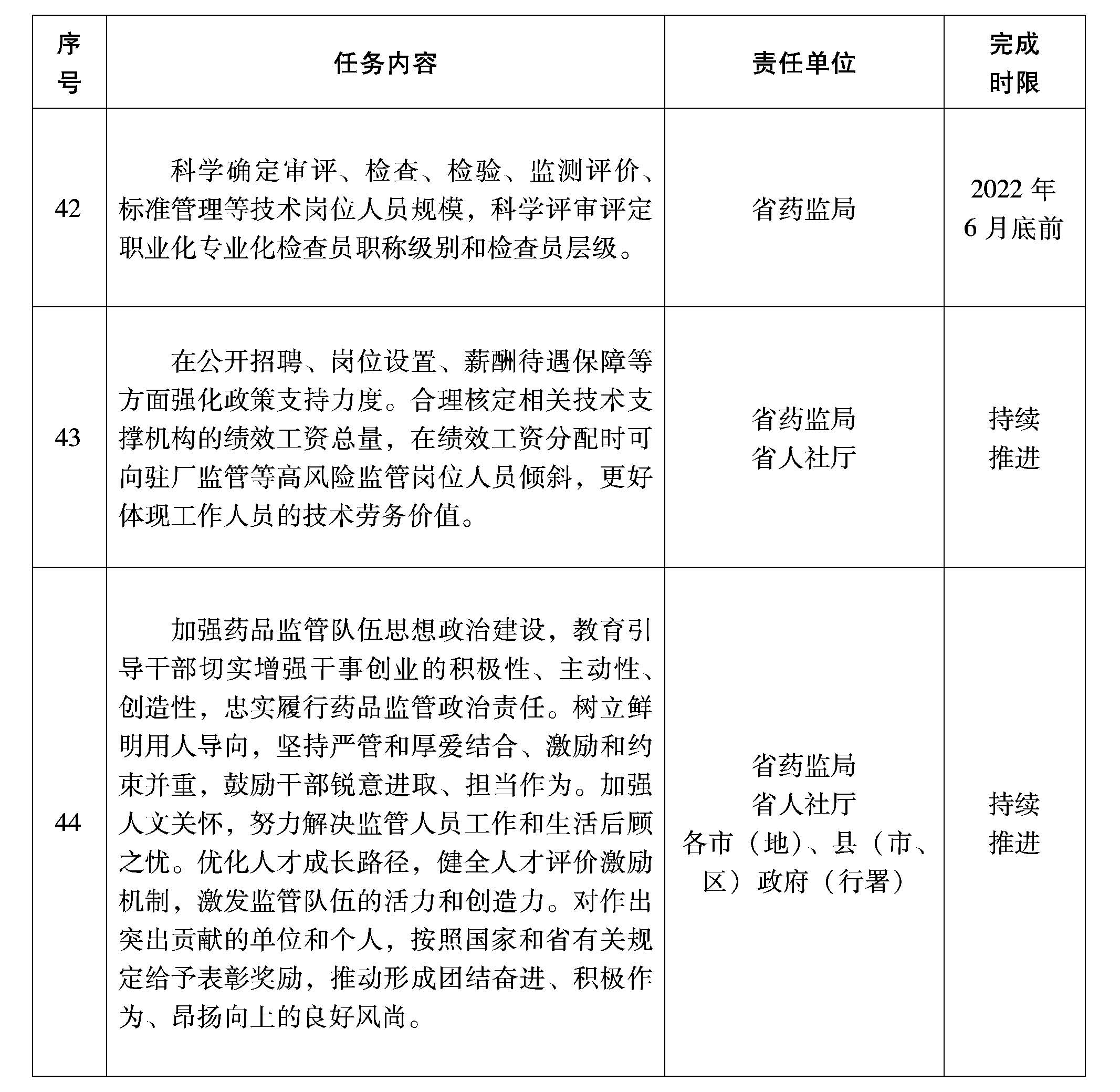
(二十二)優(yōu)化人事管理。科學確定審評、檢查、檢驗、監(jiān)測評價、標準管理等技術崗位人員規(guī)模,科學評審評定職業(yè)化專業(yè)化檢查員職稱級別和檢查員層級。在公開招聘、崗位設置、薪酬待遇保障等方面強化政策支持力度。合理核定相關技術支撐機構(gòu)的績效工資總量,在績效工資分配時可向駐廠監(jiān)管等高風險監(jiān)管崗位人員傾斜,更好體現(xiàn)工作人員的技術勞務價值。
(二十三)激勵擔當作為。加強藥品監(jiān)管隊伍思想政治建設,教育引導干部切實增強干事創(chuàng)業(yè)的積極性、主動性、創(chuàng)造性,忠實履行藥品監(jiān)管政治責任。樹立鮮明用人導向,堅持嚴管和厚愛結(jié)合、激勵和約束并重,鼓勵干部銳意進取、擔當作為。加強人文關懷,努力解決監(jiān)管人員工作和生活后顧之憂。優(yōu)化人才成長路徑,健全人才評價激勵機制,激發(fā)監(jiān)管隊伍的活力和創(chuàng)造力。對作出突出貢獻的單位和個人,按照國家和省有關規(guī)定給予表彰獎勵,推動形成團結(jié)奮進、積極作為、昂揚向上的良好風尚。
附件:《黑龍江省全面加強藥品監(jiān)管能力建設的若干措施》重點任務清單